- Historia przedmiotów
- Ogólne właściwości cyny
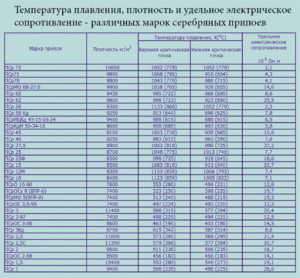
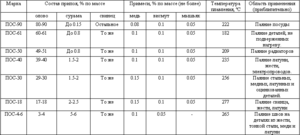
- Stopy na bazie cyny
- Korzystanie z elementu i jego połączeń
- Wpływ związków cyny
 Cyna to miękki srebrno-biały metal. Jest tak plastyczny i giętki, że jego arkusze o grubości jednej tysięcznej milimetra można zwinąć w rurkę. Taki materiał nazywa się cyną. W układzie okresowym pierwiastków D. I. Mendelejewa element ten odpowiada liczbie 50, masie atomowej 118, 69 i znakowi „Sn” (z łacińskim stannum). Znanych jest 10 jego stabilnych izotopów. Metal pozyskiwany jest głównie z minerału kasiterytu, którym jest dwutlenek cyny.
Cyna to miękki srebrno-biały metal. Jest tak plastyczny i giętki, że jego arkusze o grubości jednej tysięcznej milimetra można zwinąć w rurkę. Taki materiał nazywa się cyną. W układzie okresowym pierwiastków D. I. Mendelejewa element ten odpowiada liczbie 50, masie atomowej 118, 69 i znakowi „Sn” (z łacińskim stannum). Znanych jest 10 jego stabilnych izotopów. Metal pozyskiwany jest głównie z minerału kasiterytu, którym jest dwutlenek cyny.
Do lutowania stosuje się głównie metal w stopie z ołowiem. Ponadto jest stosowany jako powłoka antykorozyjna do pojemników ze stali spożywczej, ponieważ jest nietoksyczny. Kompozyty z cyną są stosowane jako fungicydy, farby, pasta do zębów (SnF2) i ceramika.
Historia przedmiotów
 Ten element został odkryty w 1854 roku przez Halyusa Pelegrina. Jednak jego użycie rozpoczęło się na długo przed tą datą na Bliskim Wschodzie i na Bałkanach około 2000 rpne. W tamtych czasach odkryto brąz (stop cyny i miedzi), który nadał mu nazwę Epoka Brązu. Wyprodukowali bronie i narzędzia z brązu, które były bardziej skuteczne niż kamień i kość.
Ten element został odkryty w 1854 roku przez Halyusa Pelegrina. Jednak jego użycie rozpoczęło się na długo przed tą datą na Bliskim Wschodzie i na Bałkanach około 2000 rpne. W tamtych czasach odkryto brąz (stop cyny i miedzi), który nadał mu nazwę Epoka Brązu. Wyprodukowali bronie i narzędzia z brązu, które były bardziej skuteczne niż kamień i kość.
W czasach starożytnych produkcja brązu doprowadziła do rozwoju handlu między różnymi krajami. Istnieją również odniesienia do tego metalu w Starym Testamencie. Tak więc w Mezopotamii zrobili broń z brązu, aw starożytnym Rzymie pokryli cynę wewnętrzną powierzchnię miedzianych naczyń, aby zwiększyć ich odporność na korozję.
Ogólne właściwości cyny
Wszystkie właściwości tego metalu można podzielić na dwie duże grupy : fizyczną i chemiczną.
Cechy fizyczne
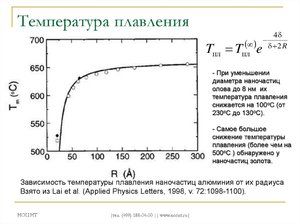 Jest to metal ciągliwy ze srebra, który łatwo utlenia się w temperaturze otoczenia, a kolor cyny zmienia się na ciemnoszary. Po zgięciu płyty z tego metalu można usłyszeć charakterystyczny dźwięk, tak zwany „krzyk cyny”, który powstaje w wyniku tarcia między jego składowymi kryształami. Jedną z jego wyraźnych cech jest gwałtowne pogorszenie właściwości mechanicznych w pewnych warunkach, zwane „plagą cyny”: poniżej -18 ° C metal ulega zniszczeniu i zaczyna wyglądać jak szary proszek.
Jest to metal ciągliwy ze srebra, który łatwo utlenia się w temperaturze otoczenia, a kolor cyny zmienia się na ciemnoszary. Po zgięciu płyty z tego metalu można usłyszeć charakterystyczny dźwięk, tak zwany „krzyk cyny”, który powstaje w wyniku tarcia między jego składowymi kryształami. Jedną z jego wyraźnych cech jest gwałtowne pogorszenie właściwości mechanicznych w pewnych warunkach, zwane „plagą cyny”: poniżej -18 ° C metal ulega zniszczeniu i zaczyna wyglądać jak szary proszek.
Czysta cyna ma dwie alotropowe modyfikacje: szarą i białą. Szara modyfikacja ma sześcienną krystaliczną strukturę, jest półprzewodnikiem, bardzo delikatnym, ma niską gęstość i jest stabilna w temperaturach poniżej 13, 2 ° C. Biała modyfikacja alotropowa ma tetragonalną strukturę krystaliczną, dobrze przewodzi prąd elektryczny i jest stabilna w temperaturach powyżej 13, 2 ° C.
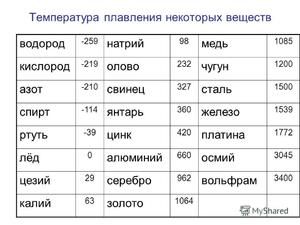
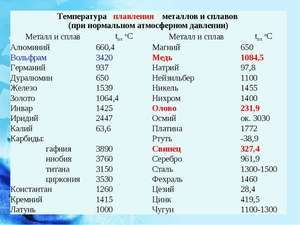
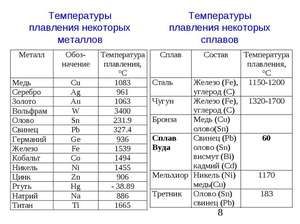
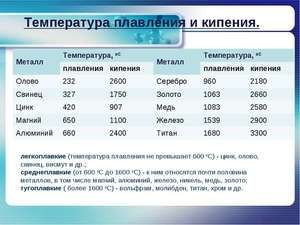
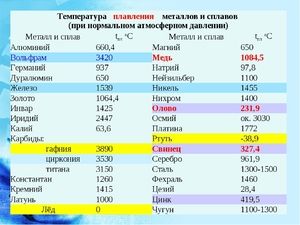
Metal topi się w stosunkowo niskiej temperaturze 232 ° C (dla porównania: żelazo topi się w 1535 ° C). Trzeba zrozumieć, odpowiadając na pytanie, w jakiej temperaturze topi się cyna, czym dokładnie jest topienie białej alotropowej modyfikacji. Pomimo niskiej temperatury topnienia wrzenie metalu zachodzi w stosunkowo wysokiej temperaturze 2602 ° C (żelazo wrze w temperaturze 2750 ° C).
Właściwości chemiczne
 Najważniejszym minerałem jest kasiteryt, SnO2. Jednak obecnie nieznane złoża rudy o wysokim odsetku tego minerału. Większość kazeitów na świecie wydobywana jest z złóż aluwialnych niskiej jakości. Z tego minerału cyna jest produkowana na skalę przemysłową. W tym celu kasiteryt jest kruszony w celu uzyskania jego koncentratu, a następnie topiony razem z koksem, kwarcem i wapnem w wielkim piecu. Następnie odlewy w postaci bloków przechodzą końcowe czyszczenie z zanieczyszczeń bizmutu, miedzi i żelaza.
Najważniejszym minerałem jest kasiteryt, SnO2. Jednak obecnie nieznane złoża rudy o wysokim odsetku tego minerału. Większość kazeitów na świecie wydobywana jest z złóż aluwialnych niskiej jakości. Z tego minerału cyna jest produkowana na skalę przemysłową. W tym celu kasiteryt jest kruszony w celu uzyskania jego koncentratu, a następnie topiony razem z koksem, kwarcem i wapnem w wielkim piecu. Następnie odlewy w postaci bloków przechodzą końcowe czyszczenie z zanieczyszczeń bizmutu, miedzi i żelaza.
Cyna pierwiastków chemicznych dobrze reaguje zarówno z mocnymi kwasami, jak i mocnymi zasadami, ale jest stosunkowo obojętna w obojętnych roztworach. Jest skorodowany w obecności czynników utleniających, przy braku tlenu metal praktycznie nie ulega korozji. Podczas utleniania na powierzchni metalu tworzy się gęsta warstwa tlenku, która chroni resztę przed dalszym utlenianiem.
 Jeśli po rozpuszczeniu soli w wodzie powstanie kwaśne środowisko, wówczas w obecności środków utleniających lub powietrza cyna reaguje. Takie sole obejmują chlorki, na przykład glin i żelazo. Większość cieczy niewodnych, takich jak oleje i alkohole, praktycznie nie reaguje z cyną. Sama cyna i jej proste sole nieorganiczne nie są toksyczne, jednak niektóre kompozyty organiczne są toksyczne.
Jeśli po rozpuszczeniu soli w wodzie powstanie kwaśne środowisko, wówczas w obecności środków utleniających lub powietrza cyna reaguje. Takie sole obejmują chlorki, na przykład glin i żelazo. Większość cieczy niewodnych, takich jak oleje i alkohole, praktycznie nie reaguje z cyną. Sama cyna i jej proste sole nieorganiczne nie są toksyczne, jednak niektóre kompozyty organiczne są toksyczne.
Tlenek cyny (II), SnO jest czarno-niebieskim kryształem, który rozpuszcza się w kwasach i zasadach. Służy do produkcji soli do galwanizacji i produkcji szkła. Tlenek cyny (IV), SnO2 jest białym pyłem nierozpuszczalnym w kwasach. Jest stosowany jako niezbędny składnik do barwienia w różowej, żółtej i brązowej ceramice, a także w dielektrykach i stopach ogniotrwałych. Jest ważnym środkiem do polerowania marmuru i innych kamieni ozdobnych.
Chlorek cyny (II), SnCl2 jest głównym składnikiem kwasu cyny do lutowania. Chlorek cyny (IV), SnCl4 jest stosowany jako składnik chemiczny w celu nadania ciężaru jedwabnej tkaninie, a także w celu stabilizacji niektórych produktów perfumeryjnych i ustabilizowania koloru mydła, a SnF2, który jest biały i rozpuszczalny w wodzie, jest stosowany jako dodatek do past do zębów.
Organicznymi związkami chemicznymi opartymi na tym pierwiastku są te związki, w których obecne jest co najmniej jedno wiązanie cyna-wodór, Sn-H, i w których metal wykazuje stopień utlenienia +4. Związki organiczne, które znalazły zastosowanie w przemyśle, mają następujące wzory chemiczne:
- R4Sn;
- R3SnX;
- R2SnX2;
- RSnX3.
Tutaj R oznacza grupę organiczną, na przykład metyl, etyl, butyl i inne, a X jest pierwiastkiem nieorganicznym, na przykład, chlor, tlen, flora i inne.
Stopy na bazie cyny
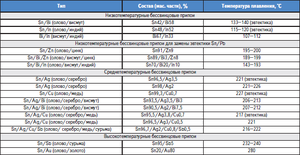 Stopy na bazie cyny są również znane jako metale białe, zwykle zawierające miedź, antymon i ołów. Stopy mają różne właściwości mechaniczne w zależności od ich składu.
Stopy na bazie cyny są również znane jako metale białe, zwykle zawierające miedź, antymon i ołów. Stopy mają różne właściwości mechaniczne w zależności od ich składu.
Cyna i stopy ołowiu znalazły komercyjne zastosowanie w szerokiej gamie związków. Tak więc 61, 9% cyny i 38, 1% ołowiu odpowiada składowi eutektycznemu, którego stopień zestalenia wynosi 183 ° C. Stopy o różnym stosunku tych metali topią się i krystalizują w szerokim zakresie temperatur, gdy występuje równowaga między fazą stałą a fazą ciekłą. Przy takiej krystalizacji segregacje stałe zaczynają się wytrącać w stopie, co prowadzi do tworzenia różnych struktur. Stop eutektyczny, ponieważ ma najniższą temperaturę topnienia, służy jako ochrona przed przegrzaniem elementów elektronicznych.
Istnieją również stopy, w których oprócz tych metali obecna jest niewielka ilość antymonu (do 2, 5%). Głównym problemem stopów na bazie cyny i ołowiu jest ich negatywny wpływ na środowisko, dlatego niedawno opracowano ich zamienniki, w których nie stosuje się ołowiu, na przykład stopów ze srebrem i miedzią.
Stopy cyny z ołowiem i antymonem są używane do biżuterii dekoracyjnej, a niektóre stopy cyny, miedzi i antymonu są stosowane jako środki smarne w celu zmniejszenia tarcia w łożyskach ze względu na ich właściwości przeciwcierne. Oprócz powyższych stopów cynę stosuje się w stopach brązu oraz w stopach z tytanem i cyrkonem.
Korzystanie z elementu i jego połączeń
Wszystkie obszary produkcji ludzkiej, w których ten element jest bezpośrednio lub pośrednio wykorzystywany, są wymienione poniżej:
 Ochrona przed korozją i naprężeniami mechanicznymi stali i innych metali, na przykład przy produkcji puszek;
Ochrona przed korozją i naprężeniami mechanicznymi stali i innych metali, na przykład przy produkcji puszek;- Zmniejszenie kruchości szkła, a także w produkcji luster;
- W pogoni za wzorami na różnych potrawach;
- Stosuj w fungicydach, farbach, pastach do zębów i różnych pigmentach.
- Po otrzymaniu różnych stopów, na przykład brązów.
- Do lutowania w niskiej temperaturze lub miękkiego;
- Złożony z ołowiu w produkcji blach do instrumentów muzycznych;
- Poprzez produkcję etykiet różnych produktów;
- W stopach chroniących przed przegrzaniem aparatury elektrycznej i mikroukładów elektronicznych;
- W przemyśle ceramicznym do produkcji emalii jako środka matującego.
- W kapsułkach do korkowania butelek wina. Produkcja takich kapsułek wzrosła po zakazie stosowania ołowiu w przemyśle spożywczym.
Wpływ związków cyny
Aktywność związków z tym pierwiastkiem, w taki czy inny sposób, wpływa zarówno na ciało ludzkie, jak i środowisko.
Na zdrowie ludzi
 Jak już wspomniano, najbardziej niebezpieczne dla zdrowia ludzkiego są organiczne związki chemiczne cyny. Substancje te są szeroko stosowane w przemyśle, na przykład w produkcji farb, tworzyw sztucznych i pestycydów dla rolnictwa. Ponadto produkcja związków organicznych z tym metalem stale rośnie, mimo że znane są konsekwencje ich zatrucia .
Jak już wspomniano, najbardziej niebezpieczne dla zdrowia ludzkiego są organiczne związki chemiczne cyny. Substancje te są szeroko stosowane w przemyśle, na przykład w produkcji farb, tworzyw sztucznych i pestycydów dla rolnictwa. Ponadto produkcja związków organicznych z tym metalem stale rośnie, mimo że znane są konsekwencje ich zatrucia .
Wpływ tych substancji na ludzi jest zróżnicowany, wszystko zależy od rodzaju związku i indywidualnych cech organizmu. Niebezpieczeństwo związku koreluje z długością wiązania między metalem a wodorem, im dłuższe to wiązanie, tym mniej niebezpieczne połączenie. Pod tym względem związek cyny z trzema grupami etylowymi, których wiązania wodorowe są stosunkowo krótkie, jest uważany za najbardziej niebezpieczną substancję organiczną.
Substancje te mogą dostać się do organizmu ludzkiego poprzez żywność, kropelki w powietrzu lub po prostu dotykając ich. Znane są następujące skutki działania organicznych związków cyny na organizm człowieka:
- W pomieszczeniu zawierającym opary tego metalu silne podrażnienie górnych dróg oddechowych, skóry i oczu;
- Bóle głowy, bóle brzucha i brak apetytu;
- Nudności i wymioty;
- Problemy z oddawaniem moczu;
- Silne pocenie się i duszność.
Wymienione efekty mogą prowadzić do poważniejszych konsekwencji:
- Depresja
- Problemy z wątrobą
- Upośledzony układ odpornościowy
- Uszkodzenie chromosomów komórkowych i brak czerwonych ciał we krwi;
- Uszkodzenie mózgu (zaburzenia snu, bóle głowy, zaburzenia pamięci, stan podrażnienia).
Do środowiska
 Zarówno atomy cyny, jak i sam metal w stanie czystym nie są toksyczne dla żadnego organizmu na ziemi, z kolei prawie wszystkie związki z tym pierwiastkiem o charakterze organicznym są szkodliwe. Związki te mogą znajdować się w środowisku przez długi czas. Są dość stabilne i praktycznie nie rozkładają się pod wpływem mikroorganizmów, ze względu na ich silne wiązania wodorowe. Bez względu na to, jak małe jest stężenie związków tego metalu w glebie i wodzie, w związku z powyższym stale rosną.
Zarówno atomy cyny, jak i sam metal w stanie czystym nie są toksyczne dla żadnego organizmu na ziemi, z kolei prawie wszystkie związki z tym pierwiastkiem o charakterze organicznym są szkodliwe. Związki te mogą znajdować się w środowisku przez długi czas. Są dość stabilne i praktycznie nie rozkładają się pod wpływem mikroorganizmów, ze względu na ich silne wiązania wodorowe. Bez względu na to, jak małe jest stężenie związków tego metalu w glebie i wodzie, w związku z powyższym stale rosną.
Wiadomo, że organiczne związki cyny wyrządzają wielką szkodę ekosystemom wodnym, ponieważ są toksyczne dla grzybów, glonów i fitoplanktonu. Fitoplankton jest ważną częścią ekosystemu wodnego, ponieważ wytwarza tlen dla wszystkich innych żywych organizmów tego układu, a także jest ważną częścią łańcucha pokarmowego. Toksyczność związków cyny jest różna dla różnych organizmów żywych, na przykład cyna tributylowa jest toksyczna dla ryb i grzybów, a cyna trifenolowa jest najbardziej toksycznym związkiem dla fitoplanktonu.
Wiadomo również, że związki organiczne tego pierwiastka mają negatywny wpływ na wzrost i funkcje reprodukcyjne zwierząt, zakłócają funkcjonowanie enzymów. Takie związki gromadzą się głównie w górnych warstwach gleby i wody.